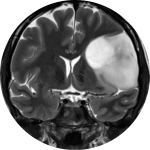
 Gliomes diffus de bas grade
Gliomes diffus de bas grade
** Imagerie métabolique
La spectroscopie-IRM mesure les principaux métabolites dans le tissu tumoral. Le spectre typique d’un GDBG montre une choline élevée, reflétant une augmentation du turnover membranaire, une diminution du N-acetyl-aspartate, reflétant la perte neuronale et une augmentation du myo-inositol, reflétant la prolifération gliale. Cependant, ces anomalies spectrales peuvent également être observées dans certaines lésions non-néoplasiques. Bien qu’il ne soit pas possible de diagnostiquer formellement le grade du gliome sur la base de la spectroscopie seule, en raison de similarités entre les gliomes de bas grade et de haut grade, la présence de lactates et de lipides (reflétant la nécrose) est associée à une plus importante activité proliférative et à un comportement plus agressif (35). L’IRM spectroscopique peut être utile pour guider la réalisation d’une biopsie, malgré les limitations déjà mentionnées, ainsi que pour le suivi longitudinal, y compris sous traitement (36).
Les séquences de perfusion-IRM DSC (dynamic susceptibility contrast imaging) permettent de calculer le volume sanguin cérébral relatif (VSCr), qui est corrélé à la micro-vascularisation. Un VCSr augmenté dans les GDBG est prédictif d’une transformation maligne avant même l’apparition d’une prise de contraste (12). Toutefois, ces observations semblent limitées aux astrocytomes, en raison d’un VCSr plus élevé dans les oligodendrogliomes.
Les séquences DCE-MRI (dynamic contrast-enhanced imaging) mesurent la perméabilité de la barrière hémato-encéphalique en calculant un coefficient de transfert (Ktrans), qui est corrélé au grade de la tumeur, même si cette corrélation n’est pas aussi forte que pour le VCSr (42).
Quant à l’IRM de diffusion, les valeurs du coefficient de diffusion apparent sont moindres et plus variables dans les oligodendrogliomes que dans les astrocytomes. Il n’y a pas de corrélation entre ce coefficient de diffusion et le taux de choline. L’IRM quantitative dans les oligodendrogliomes avec délétion 1p19q montre un signal T1- et T2- plus hétérogène, des marges moins bien délimitées et un VCSr augmenté en comparaison avec les gliomes sans délétion (6).
La tomographie par émission de positrons (TEP) peut également apporter des informations complémentaires lors du diagnostic et du suivi d’un GGII (70). La TEP au [18F]-fluorodeoxyglucose (FDG) a une valeur limitée, en raison d’une faible captation des GDBG par rapport au cortex normal. L’intérêt du PET-FDG se résume à la détection d’une transformation anaplasique dans les astrocytomes et au diagnostic différentiel entre radionécrose et récidive tumorale. La TEP à la 11C-méthionine (MET) offre l’avantage d’une captation de MET corrélée à l’activité proliférative des cellules tumorales. La captation de MET dans le tissu cérébral normal est moindre que celle de FDG, permettant un meilleur contraste et une meilleure délimitation des GDBG. De plus, les GDBG avec une composante oligodendrogliale captent davantage la MET. La TEP-MET peut être utile pour différencier les GDBG des lésions non-tumorales, pour guider les biopsies en condition stéréotaxique, pour définir le volume pré-opératoire et pour quantifier la réponse aux traitements. Un cyclotron est toutefois nécessaire.
Récemment, la 18F-fluoro-ethyl-L-tyrosine (FET) a été utilisée pour guider les biopsies et pour la planification des traitements dans les gliomes. La FET offre l’avantage d’une plus longue demi-vie que la MET, permettant ainsi la confection du traceur dans un centre avec un cyclotron et de transporter la FET dans d’autres institutions. L’expérience de la FET-TEP reste toutefois limitée par rapport à la MET-TEP, mais ce traceur semble montrer une captation et une distribution similaire dans les tumeurs cérébrales.
En synthèse, la neuroimagerie est utile pour le diagnostic, pour guider la biopsie ou la résection chirurgicale, pour planifier la radiothérapie et pour surveiller la réponse aux traitements.
 Encyclopædia Neurochirurgica
Encyclopædia Neurochirurgica

